醫療器材_產業服務

產業資訊
醫療器材產業是一先進國家與開發中崛起國家爭先投入的產業,其成長動能來自於各國老年人口數目提升及慢性疾病問題逐漸增加的人口變化因素,也是俗稱的健康商機,從產業趨勢來看,由於生技相關技術的突破與進化,讓生醫材料的應用範圍逐漸擴增,加上ICT技術的結合,也提供許多創新醫療器材的產生。產業中產品類別之產值規模為心血管相關醫材排名第一,其次依序為整形外科相關醫材、藥物輸送相關醫材、輔助類相關醫材等,B2B業務用(醫療院所)市場穩健成長,雖有些地區市場因健保或福利政策財務擴大問題會有成長沿滯現象出現,反是新興國家因中產階級崛起,業務用市場成長快速,一般此區塊是以依照醫療科別區分醫材的分類,但值得注意的是居家醫材的B2C,則隨著白色生技概念而快速成長,值得投入,這個區塊則以非侵入式的醫療器材類產品居多。
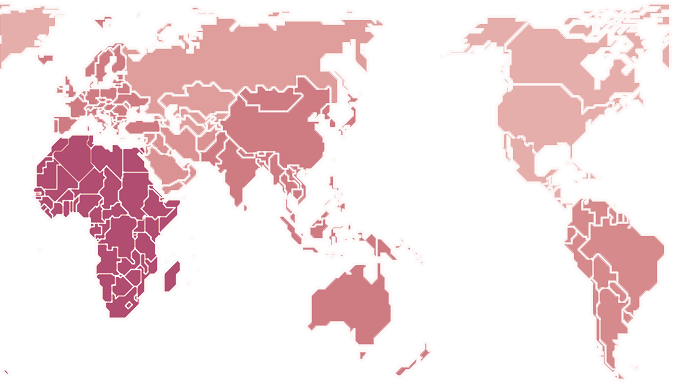
全球醫療器材市場達3,500億美元,其中生醫材料之全球市場規模達500億美元。美國仍為全球第一大市場約40%;歐盟為第二大區域市場約30%(以德英法為主);亞太成為第三大區域市場約20%(以日韓/大陸為主),如大陸市場產業規模達3,000億人民幣;台灣本身也有800億元新台幣的規模。
從商機面來看,目前診斷設備(或快速診斷技術)需求最大,尤其是體外診斷IVD,可與健康檢查掛勾,其次是與牙/骨/眼/慢性病等掛勾的醫材,而台灣目前出口的主要類別的則是輪椅類。
進入一個新市場前,您必須首先釐清該市場的產業現況,就可以採用當地第三方委託的特定產業調查服務,委託與自己進行的差別在於,從組織外的角度,更能看清利基市場,不會被過去的經驗限制,更可利用產品競爭力分析服務去了解該市場的競爭者現況與其技術水準,也應該利用專利佈局分析服務了解該市場是否有專利限制。其次應該釐清該市場的法規規範,因為醫材產品各國都有註冊登記的要求,尤其是美國及歐盟市場都有法定代理人的要求。
研發
在產品開發期間,可能會碰到許多規格設計的評估,牽涉後續終產品的安全評估,當發生疑義時,可以採取法規顧問諮詢服務的方式(service@e-sinew.com),或專案委託取得評估報告(service@e-sinew.com)。
以主要市場來說,美國FDA法規仍居全球領導地位,但其法規申辦時程(約10個月) 較歐盟申辦時程長(如英國約5個月),但歐盟法規規範較細(如醫材申報分級有6個等級)。
![]() 如果您在開發的過程,發現缺少某一特定關鍵技術,您可以透過技術交易,經由樞紐技交網來取得,也可以經由商標佈局分析服務、專利佈局分析服務與Know-how佈局來決定研究開發的方向。
如果您在開發的過程,發現缺少某一特定關鍵技術,您可以透過技術交易,經由樞紐技交網來取得,也可以經由商標佈局分析服務、專利佈局分析服務與Know-how佈局來決定研究開發的方向。
或者您開發出來的成果,也可以思考不走傳統產品供應鏈思維模式(自創品牌各國市場打仗),改為思考智財供應鏈思維模式,透過樞紐技交網交易取得授權金,授權各國廠商去打仗我們只提供子彈(智財),如果您無法判定您的智財價值,也可以透過智財評價與智財鑑價來得到答案。
組織內部研發很重要的命脈還有
一、知識管理: 知識分享環境塑造、知識文件管理、知識管理流程、知識管理系統導入輔導
二、智財管理: 智慧財產(權)管理系統(TIPS)導入輔導、智慧財產盤點輔導與營業秘密管理制度導入輔導
三、研發制度: 創意管理制度導入輔導、 研發管理制度導入輔導
上市與產品生命週期
任何產品上市後,都可能碰到消費者(或客戶)的抱怨問題,且歐美法規都規範要求業者有上市後警戒監督(vigilance)的任務,尤其是抱怨是提給主管當局時,當局是通知法定代理人(非代理商),因此要有Legal Agent(美國)及Authorized Representative(歐盟)維持與當局的溝通。
產品生命週期管理也是上市後,行銷的重要任務,在台灣可以與公協會合作,如台灣健康產業協會就是一種選項,其他包括網路行銷則應考量SEO之企業網站、網路活動設計與商品設計等作為。
如果在上市時,希望在合法的範圍內,進行最恰當的產品包裝行銷宣傳,也歡迎委託產品合法之包裝設計。