全球保健食品市場準入策略(美國 / 歐盟 / 中國大陸 / 東南亞 / 紐澳)一次看懂
保健食品業者最常見的迷思與謬誤
廣義的保健食品分成4大類,包括『機能性食品』、『膳食補充食品』、『特殊營養食品』及『健康食品』等
與我們台灣的保健食品或健康食品相比,各個國家/地區基本都有相類似的管理原則,但相關產品的名稱和定義都會有些不同,相關規範也不同。
在我們全球服務的經驗中發現
- 你以為是申請問題→其實是市場選擇錯誤。
多數企業在產品尚未確認市場適配性前,就開始詢問註冊流程與費用,但實務上,若市場選擇錯誤,即使完成所有申請,也可能面臨「無法販售」、「消費者不選擇」的結果。問題不在申請,而在一開始就選錯戰場。 - 你以為是認證問題→其實是宣稱風險。
企業常誤以為只要取得某種認證或完成登記,即可順利上市,但在美國與多數國際市場,真正影響產品能否存活的,是「宣稱是否構成誤導」。許多產品並非敗在成分,而是敗在標示與溝通方式,且通常在上市後才被放大。 - 你以為是專利技術→最常見的情況是,當產品已開發完成、包裝設計完成,甚至開始洽談通路後,才發現不符合當地法規或成分必須先被核准或宣稱不可使用。此時調整成本極高,甚至必須整個產品重來。這類問題並非個案,而是缺乏前期判斷所導致的結構性錯誤。
歡迎來信要求付費收看 2026-05-20
👉【保健食品市場趨勢與合規策略】
美國、歐盟、中國大陸、東南亞、紐澳保健食品合規一覽表
各國名稱和定義
相關產品分類與主要名稱定義我們分述於下。
- 美國:主要分類為Dietary Supplements,翻譯為膳食補充劑,功能為膳食補充之用,含有一種或多種下列膳食成分如維生素、礦物質、草本/植物功能成分、胺基酸、蛋白質等,或是以上述成分汁濃縮液/代謝物/萃取液等組合,以片狀/膠囊/錠劑/粉劑/口服液型態攝入,不以傳統食品型態出現。
- 歐盟:主要分類為Food Supplements,翻譯為食品補充劑,功能目的為針對飲食進行補充,成分可為濃縮之單一成分或複合成分,主要成分為營養素或具生理功效的物質,型態可微膠囊/錠劑/片劑/粉劑/滴劑/丸劑/口服液/安瓶等,可以小劑量攝入。
- 大陸:主要分類為保健食品(法定名詞),與台灣的健康食品相對應,必須獲得主管機關的審批核准,主要指具有特定保健功能(調節身體功能)或補充維生素/礦物質為目的的食品,不以治療疾病為目的,且對人體不產生任何急性、亞急性或慢性危害的食品。以微膠囊/錠劑/片劑/粉劑/滴劑/丸劑/口服液/安瓶型態者不得以一般食品販售。
- 日本:主要分類包括特定保健用食品、功能性標示食品及營養功能食品三類,分述如下:
特定保健用食品:指含有影響人體生理機能等保健功能成分,有助於保持正常如血壓、膽固醇、調節腸胃等標示有特定保健用途的食品(如我們的健康食品功能)。
功能性標示食品:是指基於科學依據進行生產的,不以患者為對象,通過攝取該食品中的”有效成分”,可有助於保持身體健康者。
營養功能食品:是指補充特定營養成分為目的的保健功能食品(有如大陸的保健品備案部分)。 - 南韓:主要分類為健康功能食品,是指使用功能性原料或對人體有用的原料生產加工的食品,功能性是指對人體結構或機能調節營養或提供有益的保健功能,如生理機能。
- 印度:相關分類相對複雜,主要概念是food supplements & nutraceutical,翻譯為食品補充劑與營養保健品,包含所有相關健康食品(health food)、膳食補充劑(dietary supplement)、特醫食品(food with special-medical-purposes)等相關類別,也因其印度教宗教傳統,阿育吠陀的保健品(主要是植物草藥類)也在其中,且對消費者而言,阿育吠陀認證者是主流。
- 東協:主要分類是Health Supplements,翻譯為健康補充劑,是指可以維持/增強/改善人體健康功能,用於補充飲食的產品,並含有一種或多種以下組合:1).維生素/礦物質/胺基酸/脂肪酸/酶/益生菌等生物活性物質;2).天然來源物質,包括提取物/分離物/濃縮物/代謝物形式的動物/礦物/植物物質;3).前兩項中提到的成分的合成來源。健康補充劑以小劑量單位如膠囊、片劑、粉末、液體劑型,且不包括注射劑或滴眼劑。
- 澳洲:非常特別,主要分類為Complementary Medicine,翻譯為補充藥品,顧名思義,某種程度是當成藥品管理,是指全部或部分含一種或以上特定活性成分組成的治療產品,而活性成分必須要有明確的穩定一致性與傳統的使用歷史。特定活性成分包括:1)胺基酸.2).木炭3).膽鹼鹽4).精油5).植物或草藥材料(或合成生成),包括纖維、酶、藻類、真菌、纖維素、葉綠素及其衍生物6).順勢療法製劑7).微生物或萃取物(疫苗除外)8).礦物質,包括礦物鹽和天然存在的礦物9).黏多醣10).非人體來源的動物原料,包括乾燥物、骨和軟骨、脂肪和油及其他萃取物或濃縮物11).脂質,包括脂肪酸與磷脂12).蜜蜂產生獲取自蜜蜂成分,包括蜂王漿、蜂花粉及蜂膠物質13).糖、多糖或碳水化合物14).維生素或維生素前體等。
- 紐西蘭:主要分類是Dietary Supplements,翻譯為膳食補充劑,是指1).胺基酸、可食用成分、草藥、礦物質、合成營養素或維生素2).單獨出售或以混合物形式出售3).以液體、粉末或片劑(亦可標示為4).口服用5).用於補充一般食物來源的氨基酸、可食用成分、草藥、礦物質、合成營養素或維生素。
- 加拿大:主要分類是Natural Health Product,翻譯為天然健康產品,是指用途為診斷、治療、減輕和預防疾病、精神失常等異常或疾病症狀、恢復或矯正器官功能或調節器官功能者;而原料則可包括共8類:1).植物或植物原料、藻類、細菌、真菌類或非人類動物原料;2).類別1)中所述物質的萃取物或分離物,主要分子結構與製程前相同;3).維生素(生物素、葉酸、煙酸等);4).胺基酸;5).必須脂肪酸;6).類別2)~5)所述的合成物;7).礦物質;8).益生菌。
- 台灣:主要是指健康食品(法定名詞),必須獲得主管機關的核准,具有特定保健功效,並可宣稱者。
各國相關法律法規
對於保健食品類似產品,各個國家/地區都建立了相對獨立的法律法規體系。各國保健食品類相關法律法規簡略彙整如下:
- 美國:包括[聯邦食品、藥品和化妝品法案](FD&C Act)、[膳食補充劑健康與教育法案](DSHEA)、[營養成分標籤與教育法案](NLEA)、[膳食補充劑製造/包裝/標示/儲存營運之良好作業規範(cGMP)。
- 歐盟:包括[成員國食品補充劑法](2002/46EC)、[食品營養和健康宣稱法](EC No 1924/2006)。
- 大陸:包括[保健食品註冊與備案管理辦法]、[保健食品註冊申請服務指南]、[保健食品備案工作指南]、[食品安全國家標準-保健食品](GB/6740-2014)。
- 日本:包括[健康增進法]、[食品衛生法]、[特定保健用食品審查等操作及指導要領修訂]、[營養標示基準]。
- 南韓:包括[健康功能食品法]、[健康功能食品法實施條例]、[健康功能食品法執行法令]、[健康功能食品法典]。
- 印度:包括[食品安全與標準法案](FSSA)、[營養保健品法規2016]、[標示與展示法規2018]、[特定膳食食品規範]、[食品補充劑-阿育吠陀標準]。
- 東協:包括[東協健康補充劑協議]及各國各自食品相關法規。
- 澳洲:包括[治療產品法案1989]、[治療產品法規1990]、[澳洲補充藥品法規指南]。
- 紐西蘭:[膳食補充劑法規1985]。
- 加拿大:包括[天然健康產品條例]、[天然健康產品途徑]、[天然健康產品許可申請管理]、[進行現代健康宣稱的天然健康產品許可辦法]、[作為傳統藥物使用的天然健康產品許可辦法]。
- 台灣:包括[健康食品管理法]、[健康食品法施行細則]、[健康食品申請許可辦法]、[健康食品查驗登記審查原則]。
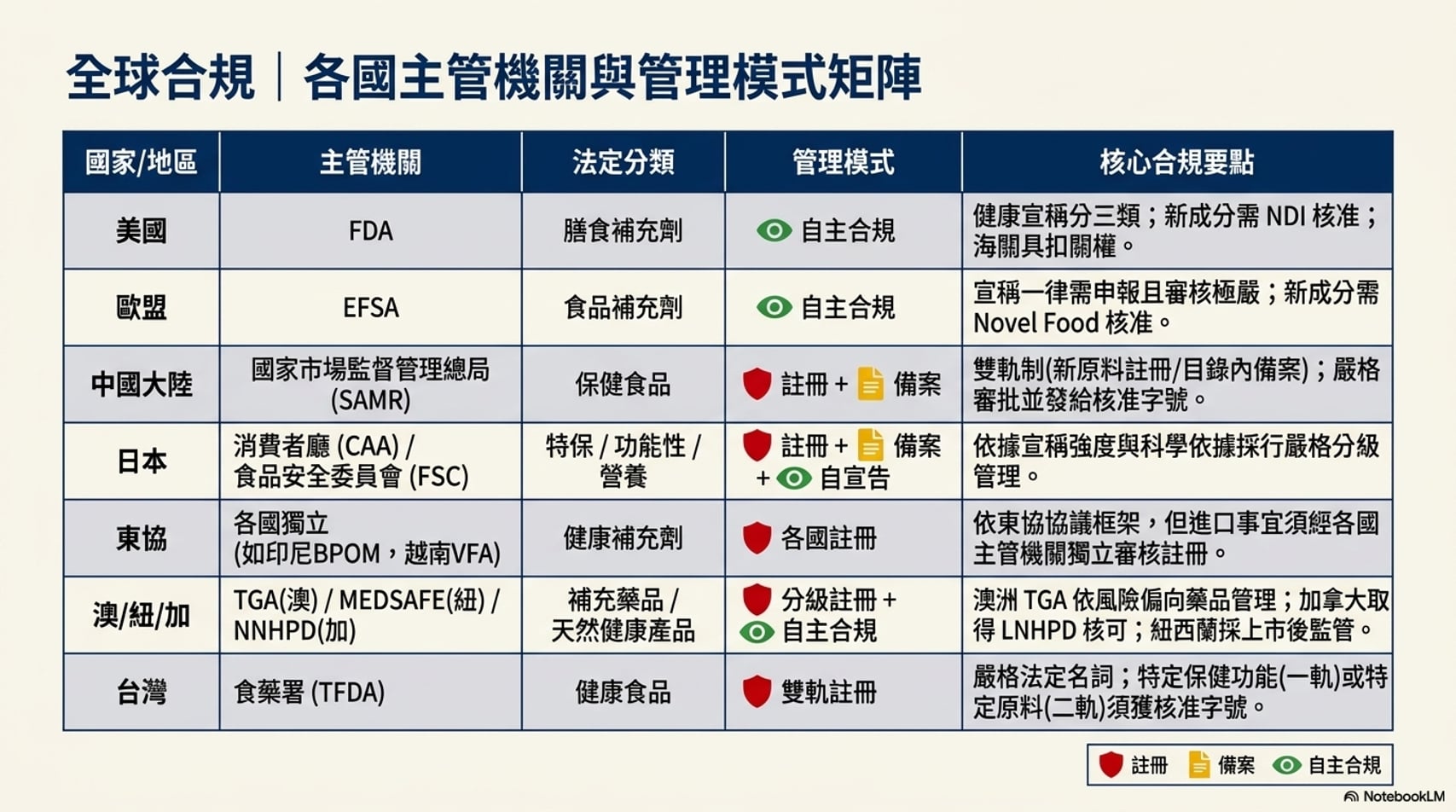
各國主管機關和管理模式
各個國家/地區的主管機關與管理模式都不盡相同,但都有主管機關,目前只有台灣與大陸都將健康食品/保健食品列入法定名詞模式實行嚴格監督管理,台灣採用一軌與二軌並行的管理模式,而大陸採用註冊與備案相結合的管理模式,日韓也有採取註冊及備案等模式。基本上,各國的類似產品的管理模式大致分為註冊管理、備案管理和自主合規這三種,我們分別簡述如下。
- 美國:主管機關為FDA。合規管理模式主要為成分自主合規(違反時海關可扣關+上市下架)與標籤自主合規(違反時海關可扣關+上市下架),但健康宣稱則分為可固定字句宣稱、特定宣稱向FDA備案及特定宣稱事先申請核准三種類別。此外,新穎性成分則需要申辦NDI的核准。
- 歐盟:主管機關為EFSA,部分國家另需要當地國之主管機關再申報。合規管理模式主要為成分自主合規(違反時海關可扣關+上市下架)與標籤自主合規(違反時海關可扣關+上市下架),健康宣稱則一律需要申報核准,且其審核較美國更嚴格。此外,新穎性成分則需要申辦novel food的核准。
- 大陸:主管機關為國家市場監督管理總局。管理模式分有註冊及備案兩種,需註冊者包括使用[保健食品原料目錄]以外之原料的產品及首次進口的非維生素/礦物質類產品;可備案者則為使用[保健食品原料目錄]內之原料及首次進口之維生素/礦物質類產品。惟使用之原料並不在過去有食用歷史的原料,應先申辦[新食品原料]的核准。核准通過者皆合發核准字號。
- 日本:主管機關為消費者廳及食品安全委員會。其中屬於特定保健用食品者必須註冊核可;屬於功能性標示食品者只需要備案;而營養功能食品則只要自我宣告即可。
- 南韓:主管機關為韓國食品與藥品安全部(MFDS)。若是特定間康功能食品必須註冊;若是一般健康功能食品則只需要備案。
- 印度:主管機關為印度食品安全與標準主管局(FSSAI)。所有保健食品都需要註冊,也可能被分類至不同的管理類別。
- 東協:東協雖然有委員會審議相關協議,但進口事宜都是各國主管機關審核,如印尼的BPOM、越南的VFA、馬來西亞的FSQD等。主要貿易國家的管理模式都是註冊(因為連一般食品都要註冊),但多數也都會追隨先進國家對產品的核准概念。
- 澳洲:主要主管機關為治療產品管理局(TGA),隸屬於Department of Health and Aged Care,其原文定義主管藥品/醫材/生物製品,但一般保健食品有健康宣稱的會被歸類由TGA管理,TGA註冊是屬於當地進口商的權責,製造廠無法擁有註冊結果,但可要求進口商註冊是連結製造商,進口商就無法改由別的製造商製造,一般決定分類分級後,會判定境外製造商是否需要被查廠。在治療產品允許使用物質列表以外的產品成分者必須註冊;若成分在列表中且屬於低風險的宣稱(符合治療產品允許宣稱列表)的產品可以備案進行;若成分在成份列表中但使用宣稱列表外的宣稱者屬於中風險則需要進行評定備案的步驟。
- 紐西蘭:主管機關為藥品與醫材安全局(MEDSAFE),特定產品需要註冊,多數產品自主合規,採用上市後監管的模式。
- 加拿大:主管機關為天然與非處方產品管理局(NNHPD),依據產品安全性及功能宣稱會進行分級註冊的概念,取得Licensed Natural Health Products Database (LNHPD)的核可。
- 台灣:主管機關為食藥署(TFDA)。也許大家相對熟悉,管理模式為特定保健功能以一軌審核程序進行核准,特定原料者可以二軌審核程序進行核准,兩者經核准皆有核准字號。
企業在選擇市場前,最先應該思考的自我檢查問題
從上述國內外保健食品類似產品的具體資訊中,我們可以看到各個國家/地區對於保健食品的概念和監管方式均有些不同。但同時也可以看到,該類產品的定位和要求確實有一些共同點,比如對產品中使用的原料有要求(尤其是安全性)、對產品的保健功能/使用目的有要求、可用劑型比較相似(多以片劑、膠囊、粉劑、口服液等劑型為主)、對該類產品的管理有相對獨立的法規體系、對該類產品的管理有專門的管理機構和管理模式等等,只是關注的重點不完全相同,很明顯的,很難用同一套實驗數據與文件想獲得各國的核准與合規,但肯定有一些可以通用的基本實驗數據,進入市場前,一定要釐清的問題有那些呢?
A:應該先選市場。多數企業是先完成配方與包裝,才開始評估市場,結果發現:
- 成分不被接受
- 宣稱不能使用
- 標示需重做
A:不是申請流程,而是「能不能合法販售與溝通」。企業常以「哪國好申請」做決策,但實務上,真正影響關鍵的是:
- 成分是否可用?
- 宣稱是否可說?
- 市場是否買單?
A:是監管邏輯,而不是名稱。
例如在美國採自主合規責任制,企業可快速上市,但需自行承擔宣稱風險與懲罰;在歐盟體系下,宣稱需審查;而在中國大陸則涉及註冊或備案。同一產品,可能在不同市場出現完全不同結果。
A:關鍵在「宣稱能不能成立」。
常見情境是: 成分都可以使用 但宣稱在某市場被視為誤導 因此產品不是不能賣,而是「不能這樣賣」。
A:不一定。實務上常見:
美國可用,但歐盟需評估新成分
歐盟可用,但美國宣稱風險高
「同一配方全球適用」在高宣稱產品中很少成立。
A:通常沒有一組單一的檢驗或認證可以適用全球各國的需要。
我們建議,完成成分與標籤針對指定國家的合規分析,最好生產廠商能夠取得NSF GMP驗證。
NSF 保健食品相關輔導服務
A:產品無法上市、無法通關或進口後無法銷售。
例如:註冊被退件、在海關被扣關、已生產產品無法銷售或已在市場上,卻涉及消費者訴訟或是被政府起訴!!
這些問題通常在投入資源後才被發現。
A:因為把產品註冊當成行政代辦「申請流程」,而不是合規風險分析與市場策略。
當產品計畫已經完成,才開始思考要找誰註冊??,通常已經太晚。
A:通常無法直接判斷。因為是否違規取決於:
- 使用語境
- 整體標示
- 主管機關如何解讀
A:風險很高。
公開資料多為原則性規範,但實務判斷涉及案例與執法方式,並非單一條文可解決。AI的部分,則如果不是專門為合規設計的AI,一般通用型AI對條文判決,會有幻覺。
A:不能只看申請費用與是否被審查。應考量:
- 配方調整成本
- 失敗機率
- 上市時間
A:不一定。 若市場條件差異大,試水溫結果可能無法轉用,甚至誤導決策。
A:需同時評估三個面向:
- 成分是否合法存在
- 宣稱是否可行
- 商業是否合理
SCG樞紐科技顧問,透過美、歐、中國大陸與東盟各地 SCG安心服務聯盟提供各國保健食品/特殊食品註冊, 歡迎瀏覽下列服務:
-
美國保健食品相關輔導服務
美國保健食品並不像台灣為註冊制(健康食品),而是須在上市前30天前完成標籤宣稱的 [輸美食品宣稱備案]
-
歐盟保健食品相關輔導服務
歐盟保健食品必須符合成分準用、標籤共通性要求,並具備市場國當地語言 [歐盟EU食品成分/標示/宣稱預審],須分別完成當地國 notification
-
大陸保健食品相關輔導服務
大陸保健食品 [批文(註冊&備案)] 分為備案制與註冊制兩種,要看是否符合原料目錄與功能目錄。
- [台灣健康食品]:註冊制,使用的原料比一般食品範圍更廣。
-
東南亞/東協/東盟保健食品相關輔導服務
包含清真制度的確認與釐清。
- [印度保健食品相關輔導服務]
- [日本/韓國保健食品相關輔導服務]
- [紐西蘭/澳洲保健食品相關輔導服務]
- [馬來西亞營養保健食品相關輔導服務]
